Chimie Organique
Molecules Organiques
et Médicinales
Des planches
BD
Les Aromatiques
© The scientific sentence. 2010
| |
|
Chimie 2:
Chimie organique
Nomenclature en Chimie organique
1. Définitions et nomenclature
Un composé organique est un composé qui contient l'élément chimique
carbone.
Une molécule organique, autre que celle d'un hydrocarbure,
est constituée d'un squelette carboné et
d'un ou plusieurs groupes caractéristiques.
• Le squelette carboné de la molécule comporte l'enchaînement des atomes
de carbone et d'hydrogène.
• Le groupe caractéristique comporte au moins un atome autre
que C et H; par exemple O, Cl, N, ....
Un hydrocarbure (HC) se compose essentiellement d'atomes de carbone et d'atomes
d'hydrogene.
Un hydrocarbure saturé désigne un hydrocarbure dont la chaîne carbonée est
constituée uniquement de liaisons simples. Exemple: les alcanes.
Un hydrocarbures insaturé désigne un hydrocarbure dont la chaîne carbonée présente
au moins une liaison double ou triple.
Exemple: les alcènes, les alcynes et les hydrocarbures aromatiques.
Un hydrocarbure acyclique est un hydrocarbure linéaire où chaque atome de carbone
n'est lié qu'au plus à deux autres atomes de carbones.
Exemple: les allènes.
Dans un hydrocarbure cyclique , la chaîne carbonée se referme sur elle-même.
C'est le cas d'un hydrocarbure alicyclique comme le cyclohexane, ou
aromatique, comme le benzène.
Un hydrocarbure ramifié désigne un hydrocarbure où un ou plusieurs atomes de carbone
sont liés à plus de deux autres atomes de carbone.
Exemple:l'isooctane.
La chaîne principale est celle qui possède le plus grand nombre de carbones.
La ramification est un substituant (ou un radical) qui est greffé à la chaîne principale.
Un radical prend une terminaison en yle.
La nomenclature permet de trouver le nom d’une molécule a partir de sa
structure, ou de trouver sa structure a partir de son nom.
2. Les hydrocarbures saturés acycliques :
les alcanes
| Nombre de C | Préfixe |
| 1 | méth |
| 2 | éth |
| 3 | prop |
| 4 | but |
| 5 | pent |
| 6 | hex |
| 7 | hept |
| 8 | oct |
| 9 | non |
| 10 | déc |
| 11 | undéc |
| 12 | dodéc |
| 13 | tridéc |
Nom :
préfixe correspondant au nombre de carbones de la chaîne + terminaison ane
Exemples
• CH3-CH2-CH2-CH2-CH3
5 carbones : préfixe pent,
HC saturé : terminaison ane
→ pentane
• CH3-CH2-CH2-CH2-CH2-CH2-CH2-CH3
8 carbones : préfixe oct,
HC saturé : terminaison ane
→ octane
3. Hydrocarbures saturés acycliques ramifiés
3.1. Numérotation de la chaîne
• Les indices indiquant l’emplacement des radicaux doivent être les plus petits possibles.
| CH3 | - | CH2 | - | CH2 | - | CH2 |
- | CH | - | CH2 | - | CH3 | |
| | | | | | | |
| | | | | | | |
| | | | | | | |
| CH3 | | | | | |
| | | | | | | |
| | | | | | |
| 1 | | 2 | | 3 | | 4 |
| 5 | | 6 | | 7 | |
| 7 | | 6 | | 5 | | 4 |
| 3 | | 2 | | 1 | |
| CH3 | - | CH2 | - | CH2 | - | CH2 |
- | CH | - | CH2 | - | CH3 | |
| | | | | | | |
| | | | | | | |
| | | | | | | |
| CH3 | | | | | |
La numérotation droite-gauche est correcte.
Nom = 3-méthylheptane
• Dans le nom, les substituants perdent le e, la terminaison est donc en
yl.
• Les substituants sont placés avant le groupe principal.
• S’il y a plusieurs groupes substituants, on les place par ordre
alphabétique, sans utiliser les préfixes multiplicateurs.
| CH3 | - | CH | - | CH2 | - | CH2 |
- | CH | - | CH2 | - | CH3 | |
| | | | | | | | |
| | | | | | | |
| | | C2H5 | | | | |
| CH3 | | | | | |
Nom =
éthyl-méthylheptane
• S’il y a plusieurs fois le même groupe dans la molécule, on utilise un préfixe
di, tri, tétra, ... pour un nombre de substituants identiques respectifs 2, 3, 4, ...
| CH3 | - | CH | - | CH2 | - | CH2 |
- | CH | - | CH2 | - | CH3 | |
| | | | | | | | |
| | | | | | | |
| | | C2H5 | | | | |
| C2H5 | | | | | |
Nom =
di-éthylheptane
3.2. Ramifications multiples
| 1 | 2 | 3 | 4 | 5
| 6 | 7 | 8 | 9 | 10 |
11 | 12 |
| CH3 | - CH2 | - CH2 | - CH
| - CH2 | - CH2 | - CH2 | - CH2 | - CH2 | - CH2 |
- CH2 | - CH3 |
| | | | |
| | | | | |
| | |
| | | | CH2
| | | | | |
| | |
| | | | |
| | | | | |
| | |
| | | | CH
| - CH2 | - CH3 | | | |
| | |
| | | | |
| | | | | |
| | |
| | | | CH2
| | | | | |
| | |
| | | | |
| | | | | |
| | |
| | | | CH3
| | | | | |
| | |
Les chaînes latérales ramifiées sont numérotées à partir du carbone lié à la chaîne principale.
• Chaîne principale (10 C) : dodécane
• Indice de substitution principal : 4
• Nom du radical ramifié :4-butyl
• Nom de la ramification secondaire : 2-éthyl
Nom =
4-(2-Éthylbutyl)dodécane
Le nom de la chaîne secondaire peut être mis entre parenthèses
lorsque c'est nécessaire.
4. Hydrocarbures insaturés acycliques
Un HC est insaturé s'il comporte une double ou triple liaison.
4.1. Hydrocarbures à doubles liaisons : les alcènes
Le nom d’un HC insaturé avec double liaison est formé par le préfixe
de l’HC saturé correspondant, où la terminaison ane devient ène.
Exemple
| 1 | 2 | 3 | 4 | 5
| 6 | 7 |
| CH3 | -CH2 | -CH | = CH | -CH2
| -CH2 | -CH3 |
• 7 C → hept
• 1 double liaison en position 4
⇒ hept-4-ène
S’il y a plusieurs doubles liaisons, la terminaison est diène , triène, ...
pour 2, 3, ... doubles liaisons respectivement.
Exemple
| 1 | 2 | 3 | 4 | 5
| 6 | 7 |
| CH3 | -CH2 | -CH | = CH | -CH2
| -CH | =CH2 |
• 7 C → hept
• 2 doubles liaisons en position 4 et 7
⇒ hept-4,7-diène
Il ya des dénomination non systématique. C'est le cas de
l'éthylène :
CH2=CH2 éthylène (et non éthène)
4.2.Substituant à doubles liaisons
Pour les composés insaturés, la chaîne principale est celle qui contient le plus d’insaturations.
La terminaison est : ényle (ényl dans le nom)
Exemple:
Le 3-propylnon-2-ène
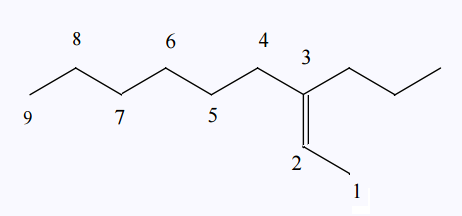
Il ya des dénominations non-systématiques:
• CH2=CH- vinyle (et non éthényle)
• CH2=CH-CH2- allyle (et non prop-2-ényle)
4.3. Hydrocarbures à triples liaisons : les alcynes
Le nom d’un HC insaturé avec triple liaison est formé par le préfixe de l’HC saturé
correspondant. La terminaison ane devient yne.
Exemples:
| 1 | 2 | 3 | 4 | 5 |
| HC ≡ | C | -CH2 | -CH2 | -CH3 |
pent-1-yne
Avec plusieurs triples liaisons :
| 1 | 2 | 3 | 4 | 5 |
| HC ≡ | C | ≡ C | - C | -CH3 |
pent-1,3-diyne
| 1 | 2 | 3 | 4 | 5 | 6 |
| HC ≡ | C | ≡ C | - C | -C |
≡CH |
hexatriyne
Dénomination non-systématique :
HC ≡ CH
acétylène (et non éthyne)
4.3.1. Substituant à triples liaisons
Terminaison : ynyle (ynyl dans le nom)
Exemples:
H3C - C ≡ C - CH2 -
but-2-ynyle
4.3.2. HC avec doubles et triples liaisons
On utilise le préfixe de l’HC saturé et une terminaison ényne.
Les liaisons multiples portent les indices les plus bas possibles.
Lorsqu'un choix se présente, la double
liaison a l’indice le plus bas.
Exemples:
| 1 | 2 | 3 | 4 | 5 |
| CH2 | = CH | - CH2 | - C | ≡ CH |
pent-1-ène-4-yne
5. Hydrocarbures monocycliques saturés et insaturés
5.1. Hydrocarbures monocycliques saturés
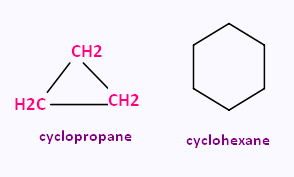
Le nom d’un HC monocyclique saturé se forme en accolant le préfixe cyclo-
au nom de l’HC acyclique saturé.
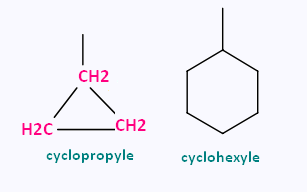
Les noms des radicaux sont obtenus en remplaçant la terminaison
ane en yle (yl dans le nom).
5.2. Hydrocarbures monocycliques insaturés
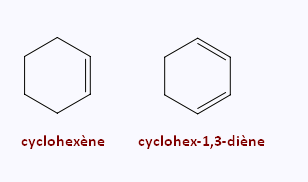
Le nom d’un HC monocyclique insaturé se forme en accolant le préfixe cyclo-
au nom de l’HC acyclique insaturé.
La terminaison se forme, comme un monocycle saturé, mais
avec une terminaison ène, diène,..., yne, diyne, etc.
5.3. Hydrocarbures monocycliques aromatiques
Un composé mono- ou polycyclique est aromatique lorsque :
1) Il possède des doubles liaisons alternées.
2) Il comprend (4n + 2) électrons π; n étant un nombre entier.
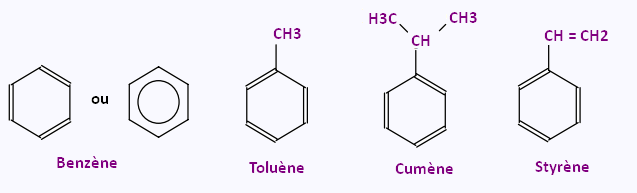
C'est l'exemple du benzène et de ses dérivées ayant
un nom non-systématique:
5.3.1. Substitution du cycle
On indiqe une substitution par des nombres.
Les substituants ont les indices les plus bas possibles.
Si un choix se présente, on considère l'ordre alphabétique.
Exemple
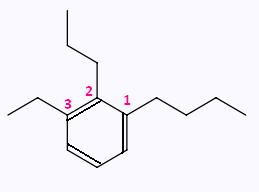
1-butyl-3-éthyl-2-propylbenzène
5.3.2. Radicaux aromatiques
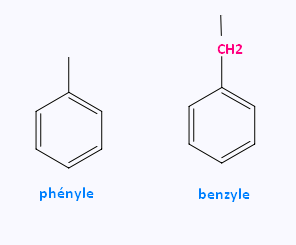
5.3.3. Polyaromatiques condensés
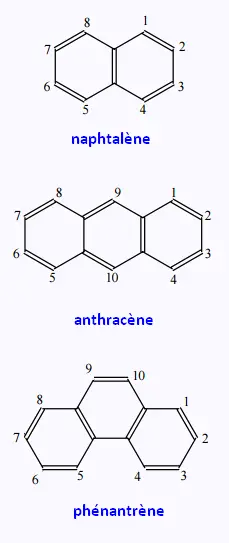
Les composés polycycliques polyaromatiques peuvent se combiner de
plusieurs fçons. Voici trois exemples de ces composés :
La numérotation se fait dans le sens des aiguilles d’une montre commence
par le carbone le plus haut dans le cycle de droite.
Les carbones communs à plusieurs cycles ne sont pas numérotés.
• Cette règle implique un positionnement correct de la molécule.
• L’anthracène fait exception à cette règle.
6. Exemples
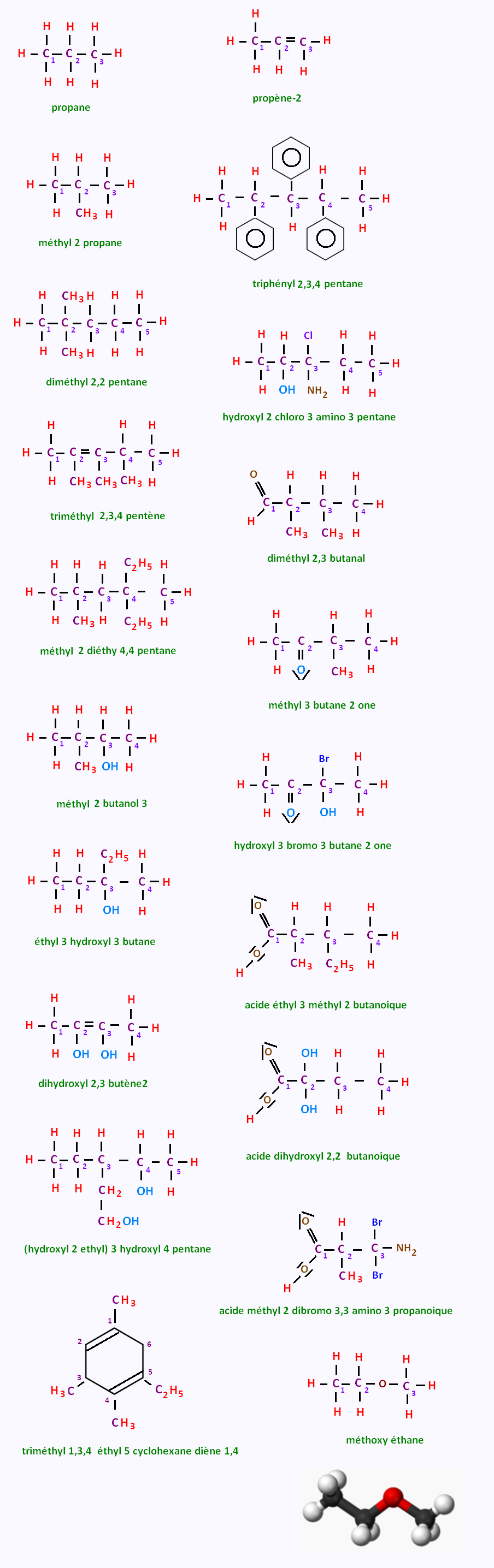
|
|