Chimie des solutions
Cinétique chimique
Distillation
Procédés de séparation
Polymérisation
Électrolyse
Traitement eau
© The scientific sentence. 2007
| |
| Chimie: Les liaisons chimiques et les molécules
Formation d'une molécule
Une molécule est une association d'atomes. Un élement
est représenté par son symbole. Une molécule est représentée
par sa formule chimique.
Exemples:
La molécule d'eau a pour formule H2O. Elle possède deux atomes
d'hydrogène et un atome d'oxygène.
La molécule d'acide sulfurique a pour formule: H2SO4.
Elle possède deux atomes d'hydrogène, un atome de soufre, et quatre atomes
d'oxygène.
Il n'existe pas de molécule dont les constituants ne figurent
pas dans le tableau périodique des élements. L'association des atomes dans une molécule
obéissent à des règles logiques et mathématiques. On ne peut avoir
une liaison chimique entre le sodium et d'argon. Le sodium
est un métal prêt à libérer un électron, tandis que l'argon est un
gaz rare qui est inerte. La liaison chimique ne fait intervenir que
les électrons périphériques ou de valence d'un atome.
Comment donc s'associent les atomes?
À partir d tableau périodique des élements, on peut classer
les liaisons chimiques en quatre grandes catégories:
- Les métaux entre eux: Liaison métallique
- Les non-métaux entre eux: Liaison covalente
- Les métaux avec les non-métaux: Liaison ioniques
- Les molécules entre elles: Liaison moléculaire
1. Liaison métallique
Dans un métal, comme le cuivre, les électrons des couches externes
de chaque atome emigrent d'un atome à un autre sans cesse, de telle sorte
que tous les électrons du métal sont libres assurant ainsi une
conductivité électrique. Ce voyage électronique assure la cohésion
des atomes dans le métal. La physique du solide explique de façon
très détaillée la nature d'une telle liaison.
2. Liaison covalente
Toujours avec les électrons des couches périphériques, une liaison covalente
met en jeu un doublet d'électrons = 2 électrons. Chaque électron vient
d'un seul atome. Le mot "co" signifie en commun. Ainsi, dans une liaison
covalente simple, chaque atome met à la disposition de l'autre un électron pour
former un doublet d'électrons à mettre en commun; c'est à dire qui appartient
aux deux atomes. Si deux atomes mettent en commun 2 doublets, la liaison
est dite covalente double. 3 doublets correspondent à une liaison
triple.
Exemples:
Exemple 1: L'atome d'hydrogène
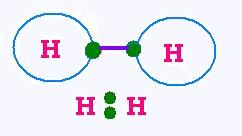 L'atome d'hydrogène posseède un électron de alence. Donc
deux atomes d'hydrogène peuvent mettre en commun un doublet
d'électrons pour devenir noble comme l'hélium. Une liaison
covalente simple entre les deux atomes s'établi.
L'atome d'hydrogène posseède un électron de alence. Donc
deux atomes d'hydrogène peuvent mettre en commun un doublet
d'électrons pour devenir noble comme l'hélium. Une liaison
covalente simple entre les deux atomes s'établi.
Ce modèle de liaison électronique fut proposé par le chimiste et physicien américain,
Gilbert Newton Lewis en 1916. On adopte désormais la notation de Lewis
pour mettre en evidence les liaisons covalentes. Les électrons de valence
se mettent vis à vis pour former des doublets. Lors d'une liaison covalente,
l'hdrogène tend à devenir hélium et tous les autres atomes tendent à acquerir des
électrons pour en avoir 8 sur leur couche externe afin de ressembler au gaz rare
le plus proche. Cette tendence à acquerir 8 électrons sur la couche externe est dite
règle de l'octet .
Exemple 2: L'atome d'oxygène
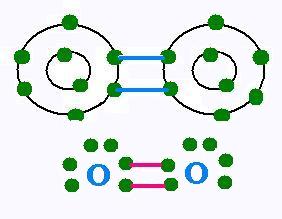 L'atome d'oxygène possède 2 électrons sur sa première couche, dite
de coeur et 6 électrons sur sa couche externe. Vis à vis, les deux atomes
d'oxygène forment une liaison covalente double. En effet, chacun
des atomes d'oxygène tend à avoir la structure du Néon, le gaz noble
qui leur est le plus proche, suivant la règle de l'octet. Une fois 2 doublets
sont mis en commun, chaque atome d'oxygène se trouve avec 8 électrons sur sa couche
de valence.
L'atome d'oxygène possède 2 électrons sur sa première couche, dite
de coeur et 6 électrons sur sa couche externe. Vis à vis, les deux atomes
d'oxygène forment une liaison covalente double. En effet, chacun
des atomes d'oxygène tend à avoir la structure du Néon, le gaz noble
qui leur est le plus proche, suivant la règle de l'octet. Une fois 2 doublets
sont mis en commun, chaque atome d'oxygène se trouve avec 8 électrons sur sa couche
de valence.
Liaison dative
Il se peut qu'un atome, lui seul, donne le doublet d'électrons
à mettre en commun pour former la liaison. Dans ce cas, cette
liaison toujours covalente est dite une liaison dative, de
coordinence ou de coordination.
3. Liaison ionique
Une liaison ionique est une liaison où les électrons ne
sont pas mis en commun, comme pour une liaison covalente. Les électrons
de valence, dans cette liaison, sout transférés d'un atome à un autre. La
régle est que ces électrons sont transférés à partir des métaux, qui
sont électropositifs aux non-métaux qui sont électronégatifs.
La liaison ionique est assurée par un transfert d'électrons
d'un atome donneur vers un accepteur. Les ions ainsi formés s'attirent par des
forces électrostatiques dites de Coulomb.
Exemple:
Un sel est, par définition, un composé ionique, c'est à dire composé
d'ions (anions et cations). Il est globalement neutre du fait que
sa charge électrique nette est nulle.
Dans un sel, comme le chlorure de sodium de formule moléculaire NaCl,
les liaisons inter-atomiques qui forment les molécules sont de type ionique.
Il faut dissoudre NaCl dans un solvant comme l'eau, pour faire apparaitre
Na+ et Cl-. Dans la molécule NaCl, dans son ensemble, les ions
Na+ et Cl- s'attirent mutuellement de sorte que
la molécule reste électriquement neutre.
La molécule NaCl
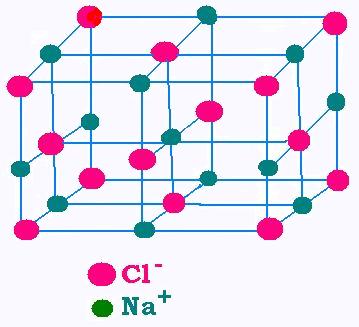 L'atome de chlorure de sodium NaCl (sel) est formée
d'un atome de sodium Na et d'un atome de Chlore Cl. Le
sodium possède 11 éléctrons, donc (11 - 2 = 9) 9 électrons
périphériques. Cet est disponible pour perdre un électron
(9 = 8 + 1) afin de ressembler au Ne qui est un gaz rare.
Il deviendra un ion (cation)sodium electropositif (Na+).
Le chlore possède 17 électrons, donc (17 - 2 - 8 = 7) 7 électrons
périphériquesest. Il est disponible pour recevoir 1 éléctron afin de
ressembler à l'argon (Ar) qui est un gaz rare. Il deviendra un ion
(anion) Chlore éléctronégatif (Cl-).
Les atomes Na et Cl dans la molécule NaCl sont liés par une liaison
purement ionique (liaison Métal-Non-métal). Cette liaison n'est
pas polaire puisque l'électron de Na est complètement transféré à Cl.
En fait, ce ne sont pas les atomes Na et Cl qui
forment la molécule NaCl; ce sont plutôt les ions Na+ et Cl-;
Ces ions de charge opposées s'attirent selon la loi de Coulomb.
La matière NaCl (chlorure de sodium) est formée d'un réseau cristallin.
L'atome de chlorure de sodium NaCl (sel) est formée
d'un atome de sodium Na et d'un atome de Chlore Cl. Le
sodium possède 11 éléctrons, donc (11 - 2 = 9) 9 électrons
périphériques. Cet est disponible pour perdre un électron
(9 = 8 + 1) afin de ressembler au Ne qui est un gaz rare.
Il deviendra un ion (cation)sodium electropositif (Na+).
Le chlore possède 17 électrons, donc (17 - 2 - 8 = 7) 7 électrons
périphériquesest. Il est disponible pour recevoir 1 éléctron afin de
ressembler à l'argon (Ar) qui est un gaz rare. Il deviendra un ion
(anion) Chlore éléctronégatif (Cl-).
Les atomes Na et Cl dans la molécule NaCl sont liés par une liaison
purement ionique (liaison Métal-Non-métal). Cette liaison n'est
pas polaire puisque l'électron de Na est complètement transféré à Cl.
En fait, ce ne sont pas les atomes Na et Cl qui
forment la molécule NaCl; ce sont plutôt les ions Na+ et Cl-;
Ces ions de charge opposées s'attirent selon la loi de Coulomb.
La matière NaCl (chlorure de sodium) est formée d'un réseau cristallin.
4. Liaison covalente polaire
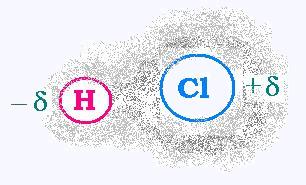 On dit covalente polaire ou simplement polaire.
On dit covalente polaire ou simplement polaire.
Dans une liaison ionique, comme celle qui lie Na et Cl pour
former le NaCl, les forces qui stabilisent cette molécule sont
de type électrostatique. Ce type de liaison se fait entre un métal et
un non-métal.
Dans une liaison covalente, comme celle dans H2, les doublets
d'électrons sont mis en commun entre les atomes concérnés. Il n'y a aucune
présence d'ion au sein de cette liaison.
Une combinaison des deux types de liaison est possible; là où la liaison
est est à la fois covalente est polaire. C'est l'exemple de chlorure
d'hydrogène (ou acide chlorhydrique) HCl. Dans cette molécule composée
d'éléments non-métaux H et Cl, liés par covalence, l'hydrogène est
électropositif et le chlore est électronégatif. Mais celui-ci est est
fortement électronégatif de telle sorte que la laison tend à devenir
ionique. Par conséquent, l'électron est beaucoup plus probable côté Chlore.
Globalement, cette présence est noté + δ pour H et - δ pour Cl.
La molécule d'eau: H2O
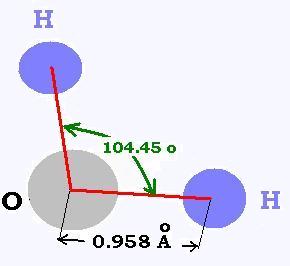 Cette molécule comporte deux atomes d'hydrogène et un
atome d'oxygène.
Cette molécule comporte deux atomes d'hydrogène et un
atome d'oxygène.
l'hydrogène consiédé come métal et l'ydrogène étant un non-métal
forment tous les deux une liaison.
L'atome d'hydrogène possède un électron et donc un électron
périphérique ou de valence. L'oxygène possède
huit électrons: 2 sur sa première couche et 6 sur sa couche de
valence (ou couche périphérique).
La règle:
Tous les atomes, au cours d'une liaison veulent être noble.
La règle du duet fait que l'atome d'hydrogène veut
gagner un électron pour en avoir deux afin de ressembler
à l'hélium qui est un gaz noble.
La règle de l'octet fait que latome d'oxygène veut
gagner deux électrons pour en avoir huit sur sa couche de
valence afin de ressembler au Néon qui est un gaz noble.
Finalement après que les deux liaisons ont eu lieu, l'hydrogène se
trouve avec 2 électrons externes et l'oxygène avec 8 électrons
externes.
Les deux liaisons H-O sont des liaisons simples covalentes et polaires.
Simple puisqu'il s'agit d'une seule liaison ( contrairement à une double
liaison), covalentes puisque la liaison met en commun un électron,
et polaire puisque l'oxygène étant très électronégatif attire
d'avantage les charges vers lui. (un exemple d'une liaison covalente non polaire
et la liaison O-O dans la molécule du di-oxygène). La molécule d'eau est polaire.
5. Notations
Nous faisons la différence entre le facteur et l'indice.
Dans
l'expression 2H2O, nous avons 2 molécules d'eau: H2O + H2O = 2H2O. Le facteur multiplicatif 2 représente le nombre de molécules.
L'indice dans H2 signifie que nous avons 2 atomes d'hydrogène H dans une molécule d'eau.
La formule chimique de la chaux s'ecrit: Ca(OH)2, composée d'un atome de calcium et de deux groupements OH, d'où l'indice 2 pour ce groupement OH mis entres parenthèses: (OH).
La formule chimique du bicarbonate de calcium s'ecrit: Ca(HCO3)2. Cette molécule comporte un atome de calcium et deux groupements bicarbonates (HCO3). Dans chaque groupement, il y a 3 atomes d'oxygène.
La règle:
Le facteur (multiplié à gauche) représente le nombre de molécules. l'indice(pondéré à droite) représente le nombre d'atomes ou de groupements dans une molécule.
Nous savons que la matière existe sous trois formes:gaz ou liquide ou solide. Nous ajoutons un autre état pour spécifier l'état de la molécule, c'est l'état aqueux qui signie "dans l'eau".
Ainsi:
H2O est liquide, on note: H2O (l),
Ca(OH)2 est solide, on note Ca(OH)2 (s),
Le dioxyde de carbone CO2 est un gaz, on note CO2 (g)
Lorsqu'une molécule est plongée dans un solvant, comme l'eau, elle porte la spécification "aqueux". La formule chimique de l'ammoniac s'ecrit: NH3 (aq) qui signifie NH3 est présente dans le solvant eau.
|