Chimie 4:
Les combustions
1. La combustion du carbone
La combustion est l'opération de bruler un corps. Le
corps brulant est un solide, liquide , ou gazeux.
1. Description de la combustion du carbone
1.1. Le carbone, qu'est ce que c'est?
Le carbone est une substance existant sous différentes forme
mais celle qui brûle le plus facilement est le fusain.
Le fusain est obtenu en chauffant, à l’abri de l’air, le bois d’un
arbuste appelé fusain. Ce chauffage permet de détruire la matière
vivante du bois et ne conserver qu’un corps pur appelé carbone.
Le charbon de bois utilisé pour les cuissons est obtenu par
le même procédé à partir d’autre type de bois. C'est un solide noir
essentiellement constitué de carbone.
1.2. Expérience: Combustion du fusain
• Etape 1:
Amorçage ou initiation de la combustion.
Initier ou amorcer une combustion consiste à la faire débuter.
On place le fusain sous une flamme (du briquet) jusqu'à ce qu'il devienne
assez chaud pour émettre une lumière rougeâtre:
le fusain est alors incandescent.
L’incandescence, c'est l'émission de lumière due à la température
d'un corps chauffé.
• Etape 2:
Combustion du fusain dans l'air
On retire le fusain de la flamme. Sa combustion se poursuit dans l'air.
Le fusain reste incandescent.
• Etape 3:
Combustion du fusain dans du dioxygène pur.
On place le fusain incandescent dans un récipient contenant
initialement du dioxygène pur.
Il se produit alors une flamme et des étincelles sont projetées.
La combustion est plus vive dans le dioxygène pur que dans l'air.
• Etape 4:
Fin de la combustion
Au bout de quelques instant la combustion devient de moins en moins
vive puis s'arrête.Une partie du fusain a disparu pendant la combustion.
• Etape 5:
Analyse du contenu du récipient où s'est réalisée la combustion:
On fait un test à l'eau de chaux dans le récipient utilisé pour la combustion:
L'eau de chaux se trouble, le test est donc positif et indique la présence
de dioxyde de carbone.
1.3. Interprétation de la combustion du carbone
• La combustion est plus vive dans le dioxygène pur
(100 % de dioxygène) que dans l’air (21 % de dioxygène):
Le dioxygène est nécessaire à la combustion du fusain.
• Dans le récipient du dioxygène pur, la combustion s'arrête
même s'il reste du fusain: c'est donc que le dioxygène disparait:
La combustion du fusain consomme donc du dioxygène.
• Une partie du fusain (de carbone) à disparu lorsque la
combustion s’arrête:
La combustion consomme du carbone.
• Lors du test à l'eau de chaux celle-ci se trouble. Ce test indique
la présence de dioxyde de carbone :
Du dioxyde de carbone s'est formé pendant la combustion.
 Conclusion :
La combustion du fusain dans le dioxygène est une transformation
chimique au cours de la quelle des corps disparaissent (du carbone et du dioxygène)
et un corps apparait (du dioxyde de carbone) . Conclusion :
La combustion du fusain dans le dioxygène est une transformation
chimique au cours de la quelle des corps disparaissent (du carbone et du dioxygène)
et un corps apparait (du dioxyde de carbone) .
2. Les transformations chimiques
2.1. Définition
On appelle transformation chimique toute transformation au cours
de laquelle des substances disparaissent et de nouvelles substances apparaissent.
Une transformation chimique peut être modélisée par une réaction chimique:
• Les substances qui disparaissent pendant une transformation
chimique sont appelées les réactifs.
• La ou les substances qui apparaissent pendant une transformation
chimique sont appelées les produits.
2.2. Exemple: la combustion du carbone.
Lors de la combustion du carbone,
Du carbone et du dioxygène disparaissent donc ce sont les réactifs.
Du dioxyde de carbone apparaît, donc c'est un produit.
On ecrit la réaction chimique de combustion du carbone comme suit:
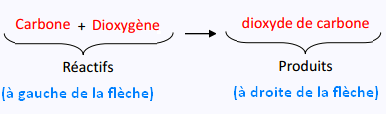
Généralement on écrit une réaction chimique selon la règle
suivante:
- Les noms des réactifs sont indiqués à gauches et séparés par un signe +.
- Les noms des produits sont indiqués à droite séparés par un signe +.
- Les noms des réactifs et ceux des produits sont séparés par une flèche
allant des réactifs vers les produits.
le signe + signifie réagit avec et la flèche pour donner.
La lecture de cette réaction chimique est donc
Le carbone et le dioxygène réagissent pour donner du dioxyde de carbone.
3. La combsution du butane
3.1. La combustion complète du butane

Expérience: On fait la combustion du butane contenu dans un briquet.
• On allume le briquet.
Pour analyser cette combustion on réalise des test:
• On place la flamme du briquet sous un tube à essais.
La paroi du récipient se couvre de buée.
La combustion se poursuit quelques instants puis la flamme disparaît
par manque de dioxygène.
On vérifie que la buée à l'intérieur du tube à essais est constituée d'eau
au moyen du test du sulfate de cuivre anhydre. Celui-ci bleuit.
On fait aussi le test à l'eau de chaux sur les gaz recueillis dans le tube
à essais. On observe que l'eau de chaux se trouble.
Interprétation : la combustion produit de l’eau et du dioxyde de carbone.
Elle consomme du dioxygène et du butane.
 Conclusion :
Les réactifs sont le butane et le dioxygène.
Les produits sont le dioxyde de carbone et l’eau.
Conclusion :
Les réactifs sont le butane et le dioxygène.
Les produits sont le dioxyde de carbone et l’eau.
Voici l'ecriture de la réaction chimique:

Cette combustion est une combustion complète.
3.2. Combustion incomplète du butane
S'il n'y a pas assez de dioxygène pour bien brûler tout
le butane il se produit une combustion incomplète:
En plus des produits indiqués il apparaît :
Un composé solide noir: du carbone
Un composé gazeux incolore, inodore et surtout très toxique:
du monoxyde de carbone
La réaction devient alors :
Butane + dioxygène → dioxyde de carbone +
eau + carbone + monoxyde de carbone
Le butane ainsi que le méthane, l’éthane et le propane
sont des gaz naturels. Chacun brûle en produisant de l’eau et du dioxyde de carbone et leur combustion peut également être incomplète.
Une combustion incomplète produit des gaz imbrûlés qui participent à la pollution de l'air.
4. Bilan sur les combustions

Les combustions sont des transformations chimiques.
Pour qu'une combustion se produise il faut réunir trois éléments:
• Un corps capable de brûler: un combustible (exemples: carbone, butane, papier, essence, etc)
• Un corps capable de faire brûler: un comburant (comme le dioxygène)
• Une source de chaleur qui permet d'initier la combustion (flamme, étincelle) puis de l'entretenir.
Si l'un de ces trois éléments manque, où si ces trois
éléments sont séparés, la combustion ne peut avoir lieu.
Pour éteindre un incendie, le pompier brise le triangle du feu,
en éliminant l'un des trois élements: le combustible, ou
le comburant , ou la chaleur.
• Avec de l'eau, Il élimine la chaleur (ignition)
• Avec le sable ou la mousse, il élimine le comburant (l'oxygène de l'air).
|