Chimie: La conductivité électrique des solutions aqueuses
1. La conductivité électrique des
solutions aqueuses
1. Test de conductivité
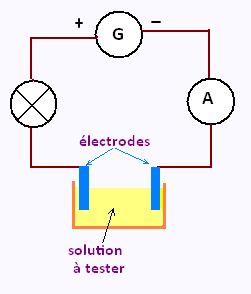
Pour savoir si une solution aqueuse est conductrice ou pas,
on lui fait subir un test.
Le test de conductivité sur les solutions aqueuses repose sur
le même principe que le test réalisé sur les matériaux solides:
La solution aqueuse est mise dans une cuve où on plonge deux tiges métalliques
appelées électrodes.
Lorsque la solution est conductrice, le courant électrique
circule et la lampe brille.
La lampe ne brille évidement que lorsque l'intensité du courant qui
la traverse est égale ou supérieure à son intensité nominale.
La lampe n'est donc pas le témoin parfait du passage du courant.
l'intensité du courant dans le circuit n'est parfois pas
suffisante pour que la circulation d'un courant électrique
soit détectée par la lampe.
Pour détecter des courants faibles on insère également dans le
circuit un ampèremètre.
Voici quelques résultats d'un test de conductivité
L'eau distillée (presque pure), l'eau du robinet, et l'eau sucrée
conduisent faiblement l'électricité. Mais l'eau salée, ainsi
que la solution de sulfate de cuivre
conduisent fortement l'électricité.
L'intensité mesurée varie donc selon les solutions testées et
selon la tension fournie par le générateur.
2. Présense des ions dans les
solutions aqueuses
conductrices
On sait que le courant électrique est un
déplacement d'électrons qui sont des particules électriquement chargées en mouvement.
Ainsi, si l'eau distillée, l'eau du robinet et l'eau sucrée sont
faiblement conductrices, alors elles contiennent très peu de charges positives.
Par contre l'eau salée, ainsi que la solution de sulfate de cuivre en contiennet
suffisament pour permettre le passage des électrons
à travers le circuit.
En effet:
• L'eau pure ne contient presque que des molécules d'eau qui
sont électriquement neutres.
• L'eau du robinet contient des molécules d'eau et des sels minéraux.
• L'eau du sucrée contient des molécules d'eau, des molécules
de sucre (molécules de saccharose) et des sels minéraux.
L'eau salée et la solution de sulfate de cuivre sont conductrices
car elles contiennent de particules électriquement chargées.
Ce sont ces particules qu'on appelle des ions.
L'eau sucrée et l'eau du robinet ne sont pas totalement isolantes
à cause de leurs sels minéraux qui sont constitués d'ions.
L'eau distillée n'est pas non plus totalement isolante car elle n'est
pas parfaitement pure: elle peut contenir, entre autres, des ions provenant
des gaz de l'air qui s'y sont dissous.
|