Chimie au cegep
Chimie & petrochimie
Chimie & laboratoires
© The scientific sentence. 2010
| |
|
Physique nucléaire: Processus de fission
et de fusion nucléaires
1. Définitions
Pour certains éléments, il peut se produire spontanément non pas une désintégration,
mais une fission nucléaire. Ce processus initialise alors plusieurs chaînes de
désintégration.
L'uranium 235, par exemple, sous l'impact d'un neutro, se transforme en deux produits
de fission qui sont le Krypton et le Barium, en émettant neutrons neutrons:
1 n + 235U → 236U → 92Kr + 141Ba +
3n
Ces trois neutrons produits serviront à leurs tours d'initialiser une deuxième
fission et ainsi de suite . C'est la réaction en chaine de l'Uranium 235.
La radioactivité est une réaction nucléaire spontanée sans aucune intervention.
Les réactions nucléaires telles que la fission et la fusion sont artificielles.
Le processus de fission est la division d'un noyau pour former deux plus petits,
alors que la fusion est la fusion de deux radioactifs plus petits pour former un plus grand.
2. Fission
2.1. Définitions
La fission est concernée par les noyaux lourds. Dans un tel procédé, un noyau, avec
un grand nombre de nucléons, capture un neutron, et se divise en deux fragments
avec un plus petit nombre de nuléons, suivi par l'émission d'un ou plusieurs neutrons.
Les deux fragments obtenus ont une faible énergie de liaison par nucléon; ils sont plus
stables en ce qui concerne le noyau initial. Le processus de fission porte essentiellement
sur les deux noyaux d'Uranium 235U , 233U , et
sur le plutonium P 239U.
Le neutron (sans charge électrique) approche un noyau sans être dévié de sa direction
par des interactions électrostatiques. Les neutrons qui ont une faible énergie cinétique
(0.1 eV correspondant à l'énergie d'un neutron à température ambiante), sont plus susceptibles
de produire la fission de 235U. Ces neutrons sont appelés neutrons thermiques.
La fission nucléaire est un processus qui nécessite des neutrons incidents pour
démarrer la réaction. Chaque neutron produit va produire un ou plusieurs autres;
donc la réaction en chaîne nucléaire a lieu. Ce processus ne dure pas longtemps.
Il dégage une forte quantité d'énergie dans un très temps court, c'est à une explosion.
Dans les réacteurs nucléaires, le processus de fission, et spécialement le taux d'émission
de neutrons, est toujours controlé.
2.2. Énergie d'une mole d'Uranium 235
La réaction d'un noyau d'uranium 235 est la suivante:
U (235,92) + n Rarr; Xe(139,54) + Sr (95,38) + 2n.
Le nombre de charge est toujours conservée.
L'énergie libérée par la réation est E = (mi - mf) c2
Nous avons pour les masses individuelles:
U(235,92): mu = 234,993 uma
Xe (139,54): MXE = 138,914 uma
Sr (95,38): MSR = 94,856 uma
n: mn = 1,009 uma
Donc:
mi = mU + mn
mf = MXE + MSR + 2mn
mi - mf = mU - MXE - MSR - mf = 0.215 uma
(environ 0.1% de la masse initiale de 235U est transformée).
E = 0.215 x 1.66 x 10-27 x 9 x 3.2 x 1016 = 3.2 x 10-11 Joules.
La grande partie de l'énergie obtenie par fission est sous forme cinétique
pour les noyaus produits, le reste est pris par les neutrons et les rayons γ.
Pour une mole, nous avons: = 6,023 x 10 23 x 3,2 x 10-11 = 2 x 1013 Joules;
ce qui est représente une quantité énorme d'énergie.
Les produits du procédé de fission sont très nombreux pour un même noyau initial. Cela est dû à
la multiplicité des modes de fission et les transformations de décomposition du noyau produit.
Pour l'235U, nous pouvons aussi avoir la réation :
U (235,92) + n → Ba (139,56) + Kr (94,36) + 3n.
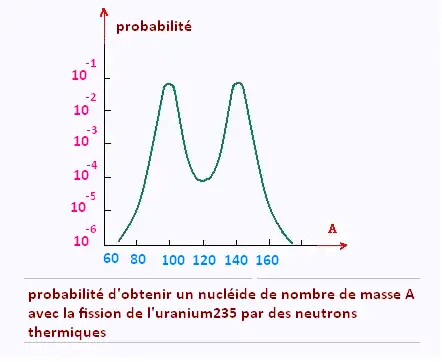
En général, la probabilité d'obtenir des noyaux par fission ressemble à celle
donné par le profil de distribution de probabilité de 235U par des neutrons
thermiques, illustré dans la figure ci_contre.
Cette courbe est légèrement modifiée lorsque les neutrons capturés sont plus énergiques.
La fission du plutonium 239 et de l'uranium 233 donne des résultats similaires.
Le plutonium 239 est un élément artificiel. Il est produit par la capture d'un neutron
d'énergie cinétique élevée (neutrons rapides) de l'ordre de quelques MeV par l'uranium 238,
suivie par l'émission de deux électrons (β-).
Par un processus identique, le thorium 232 conduit à l'uranium 233 via
le protactinium (Pa) par la série suivante:
Th (232,90) + n → Th (233,90), ensuite:
Th (233,90) → Pa (233,91) + e-, et:
Pa (233,91) → U (233,92) + e-
Le thorium 232 et l'uranium 238 sont relativeley abondant dans la nature.
Le thorium 232 conduit à uranium 233 et l'uranium 238 conduit au plutonium.239.
Ces deux produits 233U et 239Pu sont fissiles. Nous disons
que le thorium 232 et l'uranium 238 sont fertiles.
L'uranium dans la nature est composé de 0.72% d'uranium 235 fissile et 99.27%
d'uranium 238 fertile. L'uranium 238 n'est pas fissile, mais il est converti au
plutonium 239 qui est fissile comme l'uranium 235 et l'uranium 233.
2. Fusion
Dans le processus de fusion, deux radioactifs légers se combinent pour former un atome
lourd, suivie ou non par une émission particules tel que les neutrons, les électrons, les positrons, les protons, ....
Par exemple, la réaction qui se produit au soleil est:
H (1,1) + H (2,1) → H(3,2) + 3n
Comme pour une fission, une réaction de fusion conserve le nombre de nucléons et le nombre de charges.
L'énergie libérée par cette réaction est: E = (mi - mi ) c2
Nous avons pour les masses individuelles:
H (1,1): m1 = 1.0073 uma
H (2,1): m2 = 2.0134 uma
H (3,2): m3 = 3.015 uma
Donc:
mi - mf = m1 + m2 - m3 = 5.79 x 10-3 uma
E = 5.79 x 10-3 x 1.66 x 10-27 x 9 x 1016 =
8.65 x 10-13 Joules = 5.4 MeV.
La fusion est favorisée lorsque l'énergie de liaison par nucléon du noyau final est plus grande que celles des noyaux initiaux.
Pour la réaction de fusion suivante:
Li (7,3) + H (1,1) → Be(8,4),
L'énergie de liaison par nucléon pour
- le lithium est eLi = 5.4 MeV et
- le béryllium eBe = 6.8 MeV;
l'énergie libérée est calculée comme suit:
On sépare d'abord les 7 nuclons du béryllium qui nécessite l'énergie
ELi = 7 x eLi = 7 x 5.4 = 37.8 MeV.
Ensuite, On reconstitue le Be (8,4) à partir de 8 nucluons (7 de Li (7,3) et 1
de H (1,1)), qui nécessite de l'énergie EBe = 8 x eBe = 8 x 6.8 = 54.4 MeV.
D'où l'énergie libérée par la réaction est:
EBe - Eli = 54.4 - 37.8 = 16.6 MeV.
Pour réaliser celà, les nucléons initiaux doivent être très énergiques en vue de surmonter les fortes forces électriques de répultion entre les charges positives de ces nucléons.
Ainsi, la fusion nécessite des nucléons avec une énergie cinétique élevée (= 1 MeV).
La température d'un fluide augmente par rapport à l'énergie cinétique des particules constituant. Par conséquent, la fusion n'est possible qu'à température d'environ un milliard de degrés oC; qu'on appele la fusion thermonucléaire.
La fusion est spontanée dans les étoiles. Artificiellement, sur la terre, ces conditions de températures élevées pourraient être reproduites.
Cela peut déclenche la réaction:
H (2,1) + H (3,1) → He (4,2) + n
Les produits de fusion libèrent beaucoup plus d'énergie par unité de masse que
la fission. En d'autres termes, l'énergie libérée à partir d'un combustible de
1 kg d'uranium 235 est inférieure à celle d'une fusion de 1 kg de deutérium et de tritium combinés.
Actuellement, la recherche se concentre principalement sur l'obtention
d'un plasma d'une température élevée (au moins quelques dizaines de millions de degrés) et sur l'utilisation des lasers afin d'expérimenter la réaction de fusion theoriquement possible.
|