Chimie: Formation de molécules
Modèle Boules-bâtonnets
1. Se familiariser avec les couleurs
À l'aide du tableau de couleurs suivant:
| Élément | Couleur |
| Hydrogène | Blanc |
| Carbone | Noir |
| Azote | Bleu |
| Oxygène | Rouge |
| Soufre | Jaune |
| Chlore | Vert |
| Fluor | Cyan |
| Brome | Brun |
| Iode | Violet |
| Phosphore | Orange |
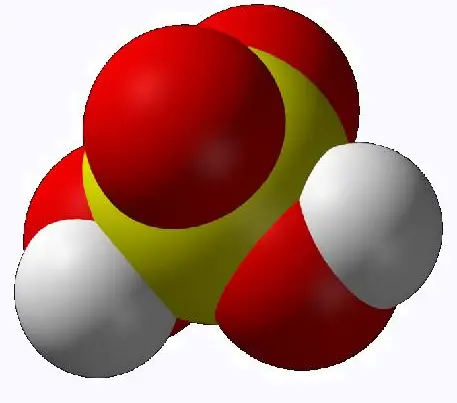
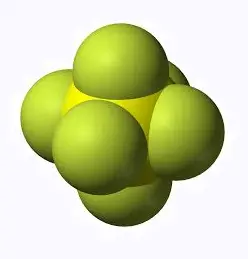
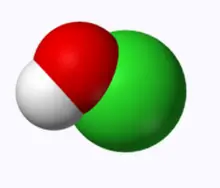
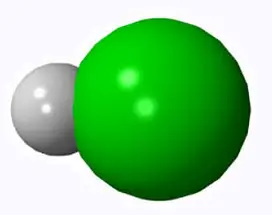
donner la formule brute
(ou structurale) des molécules suivantes:
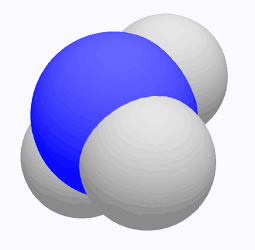
|
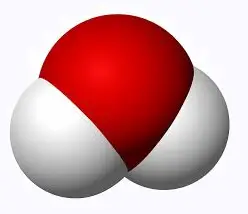
|
| 1 | 2 |
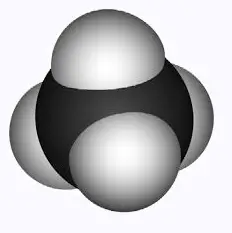
|

|
| 3 | 4 |
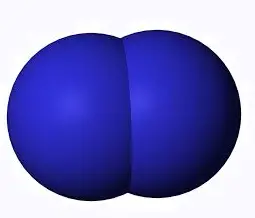
|
|
| 5 | 6 |

|
|
| 7 | 8 |

|
|
| 9 | 10 |
|

|
| 11 | 12 |
2. Équilibrage des réactions chimiques
a) Cette réaction est-elle équilibrée?
Justifier
en écrivant les coefficients stoechiométriques correspondants:
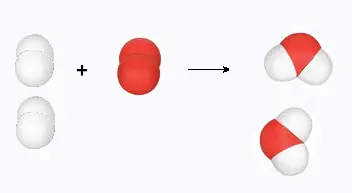
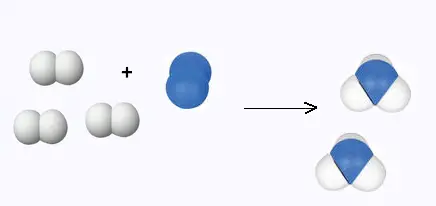
b) Équilibrer la réaction suivante qui correspond à
la formation de l'ammoniac:
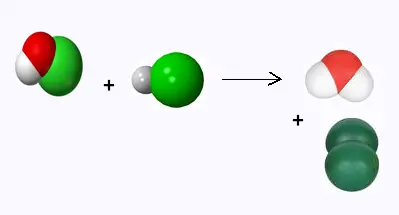
c) Dans cette réaction, si on double la quantité de l'eau de Javel (HClO)
sans changer celle de l'acide chlorhydrique, peut-on obtenir le
double de quantité d'eau?
Justifier par calcul stoechiométrique.
|