Physique
Chimie
TS
Chimie
Les acides et les bases
Applications
Mesure du pH
Équilibre chimique
Applications
Exercices résolus
Spectroscopie
RMN du Proton
Applications
Exercices résolus
Propagation
du signal
Mécanique
© The scientific sentence. 2010
|
Chimie 5:
Spéctroscopie
Chimie organique
RMN du proton
Analyse de spectres RMN
Analyse de spectres RMN
Voici la méthode pour attribuer son spectre de RMN à une molécule :
• repérer dans la molécule les groupes de protons équivalents
(le nombre de groupes est égale au nombre de signaux),
• déterminer les protons qui sont couplés (par voisinage) et en déduire la
forme des signaux en appliquant la règle de la multiplicité des (n+1)uplet,
• déterminer le nombre de protons correspondant à chaque signal
grâce à la courbe d’intégration,
• à partir du graphe, attribuer son déplacement
chimique à chaque groupe de protons de la molécule,
• vérifier à l’aide de la table de données que les déplacements
chimiques correspondent bien aux groupes caractéristiques.
Remarque
Lorsque des protons sont proches d’un groupe électronégatif (C=O, -NH-, -NH2, -OH, -O-),
leur déplacement chimique peut-être supérieur à celui indiqué dans les tables de données.
Applications
Application 1
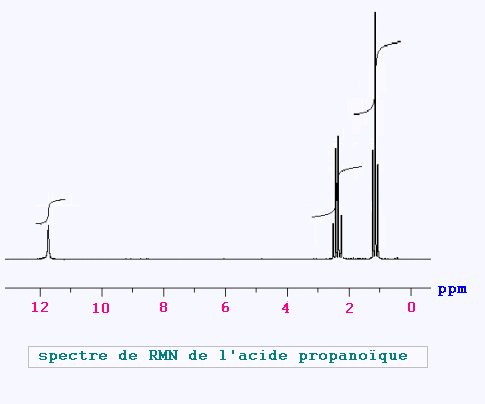
Le spectre de RMN d’une espèce de formule
brute C3H6O2 est donné ci-dessus.
Cette espèce peut-elle être l’acide
propanoïque ?
L’acide propanoïque a pour formule semi-développée :
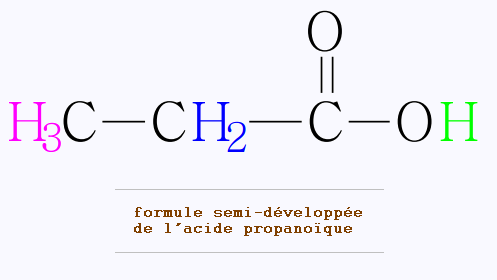
• Il y a trois groupes de protons équivalents différents
repérés en magenta, bleu et vert : le spectre de l’acide propanoïque
comporte trois signaux.
• Les protons repérés en magenta et en bleu sont couplés.
Le signal représentant les protons du groupe méthyle doit donc être
un triplet (2+1=3) et celui du groupe méthylène un
quadruplet (3+1 = 4).
• Le proton du groupe carboxyle ne se couple pas.
Son signal est un singulet.
Le spectre comporte donc un singulet, un triplet et
un quadruplet.
• La courbe d’intégration du
singulet mesure 0.4 cm,
celle du triplet 1.2 cm, et
celle du quadruplet 0.8 cm.
Donc les 6 protons de la molécule sont représentés par
0.4 + 1.2 + 0.8 cm = 2.4 cm. Soit 0.4 cm par proton.
Le singulet représente donc un proton avec δ ≈ 11.8 ppm,
le triplet représente trois protons avecδ ≈ 1.2 ppm,
et le quadruplet représente deux protons avec δ ≈ 2.2 ppm.
En utlsant la table de données, on trouve que
les déplacements chimiques sont :
- compris entre 8,5 ppm et 13 ppm pour –CO-OH,
- environ égal à 2,2 ppm pour –C-CH2-COOR,
- environ égal à 0,9 ppm pour CH3-C
Le spectre est donc celui de l’acide propanoïque.
Application 2
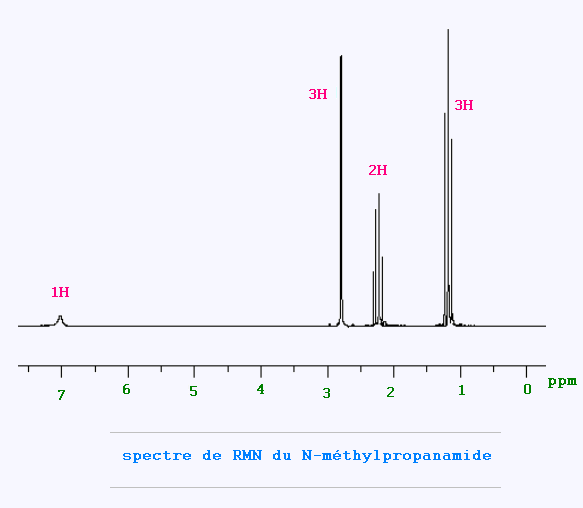
Le spectre de RMN du N-méthylpropanamide a pour formule
brute C4H9NO est donné ci-dessus.
Montrons que ctte espèce peut être le N-méthylpropanamide :
Le N-méthylpropanamide a a pour formule semi-développée :
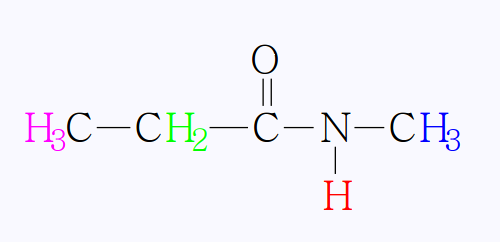
Il y a quatre groupes de protons équivalents différents
repérés en magenta, bleu, rouge et vert : le spectre comporte quatre
signaux.
• Les protons repérés en magenta et en vert sont couplés.
Le signal représentant les protons du groupe méthyle doit donc être
un triplet (2+1) et celui du groupe méthylène un quadruplet (3+1).
• Les protons du groupe méthyle et celui fixé sur l’azote ne sont pas
couplés car le proton N-H ne se couple pas.
• Le signal du groupe méthyle est un singulet, celui du proton de
l’azote est aussi un singulet.
Le spectre du N-méthylpropanamide comporte deux singulets, un triplet et
un quadruplet, comme dans le spectre présenté.
• Le quadruplet représente les deux protons du groupe méthylène avec δ = 2.2 ppm ;
- le triplet qui représente trois protons est celui du groupe méthyle avec δ = 1.2 ppm ;
- le singulet qui représente trois protons est celui du groupe méthyle porté par
l’azote avec δ = 2.8 ppm ; et enfin,
- le singulet qui représente un proton est celui du proton porté par l’azote avec ? = 7,0 ppm.
En utilisant la table de données, on trouve que les déplacements chimiques sont :
- entre 5 ppm et 8,5 ppm pour R-CO-NH,
- environ égal à 2,3 ppm pour CH3-N,
- environ égal à 1,9 ppm pour, CH2–CO-
- environ égal à 0,9 ppm pour CH3-CIl
On note que le déplacement chimique du groupe CH3-N soit supérieur à
celui donné dans les tables en raison de la présence du carbonyle C=O ;
de même celui du groupe CH2–CO- en raison de la présence de l’atome d’azote.
Le spectre est donc celui du N-méthylpropanami
|
|